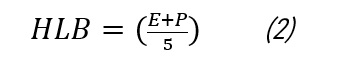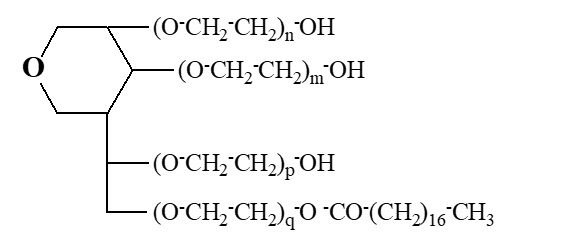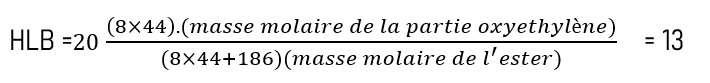Tensioactifs – partie 2
Par Aziz Lallam – Abdelaziz.lallam@uha.fr – ENSISA, 11 rue Alfred Werner 68093 Mulhouse
Introduction
Nous avons vu dans la première partie de cet article consacrée à la définition des agents de surface en général et à la classification des tensioactifs selon des critères précis [1]. La structure, la polarité de la molécule de l’agent tensioactif, la concentration micellaire critique, la tension et l’énergie de surface sont à la base de cette classification. Les spécialistes des tensioactifs s’appuient sur ces données pour rédiger les modes opératoires de chaque type de tensioactif. En revanche, l’utilisateur lambda des tensioactifs n’a pas besoin de faire appel à ces critères pour les employer dans l’une ou l’autre des applications. La simple connaissance de la valeur de la balance hydrophile- lipophile suffit pour choisir le bon tensioactif pour l’application envisagée.
Dans la seconde partie de notre article, nous allons nous focaliser sur le calcul de la balance hydrophile – lipophile HLB des agents tensioactifs.
Calcul de la HLB
Le critère d’efficacité d’un tensioactif est directement lié au degré de sa solubilité, à la fois, dans la phase aqueuse, hydrophile, et dans la phase organique, lipophile. La solubilité de tout agent tensio-actif est donc caractérisée par sa balance hydrophile-lipophile (HLB).
Selon la valeur de la balance (HLB), les tensioactifs peuvent être mouillants, moussants, détergents, lubrifiants, anti-mousse etc. L’emploi de ces produits est courant dans l’industrie textile [1] notamment dans le domaine de l’ennoblissement en tant qu’agent mouillant dans les prétraitements et dans la teinture. Parfois, ils sont utilisés en tant qu’agent anti-mousse [2] et toujours en tant que détergent dans les opérations de lavage industriel.
La phase dans laquelle l’émulsifiant est le plus soluble constitue la phase continue de l’émulsion. Par exemple, un émulsifiant soluble dans l’eau a le pouvoir de stabiliser une émulsion de type huile dans eau et inversement. Les valeurs de la HLB s’échelonnent de 0 à 20 et, plus la HLB est élevée plus l’émulsifiant est hydrophile. Nous présentons, dans la suite de cet article, les différentes méthodes de calcul de la HLB.
Méthode 1.
Des lois empiriques ont été élaborées pour calculer les valeurs de la HLB de la plupart des tensioactifs disponibles. On peut, par exemple, calculer la valeur de la HLB d’un tensioactif de type ester d’acide gras et d’un alcool polyhydroxylé par la relation de Griffin [2] dont l’expression est la suivante :
Dans cette expression, S représente l’indice de saponification de l’acide gras et le terme A est l’indice d’acide. La HLB varie entre 0 totalement hydrophobe et 20 entièrement hydrophile. L’application de la relation de Griffin permet de calculer, par exemple, la HLB du monostéarate de glycérol (1-stéaryl sn glycérol). En reprenant les valeurs de la littérature pour l’indice de saponification, 154,4 et de l’indice d’acide, 197,1[3] que l’on injecte dans l’équation de Griffin comme indiqué ci-dessous :
HLB = 20 (1- 154,4/197,1) = 20 (1-0,79) = 4,2
La valeur 4.2 indique qu’il s’agit d’une molécule hydrophobe capable de stabiliser une émulsion eau dans huile, voir tableau 2, annexe 1.
Méthode 2.
Lorsque l’indice de saponification n’est pas disponible ou difficile à obtenir, on aura recours à l’expression empirique 2 pour le calcul de la HLB comme suit :
Dans le cas d’un alcool polyhydroxylé, E représente le pourcentage de fonctions oxyéthyléniques et P, le pourcentage d’alcool polyhydroxylé (Cf. Schéma ci-dessous)
Dans le cas du polysorbate, figure ci-dessus, si les valeurs de n, m, p et q sont prises comme étant identiques et égales à l’unité, E est estimé à 29% et P à 8%. La valeur de la HLB est calculée comme suit :
HLB = (29 + 8)/5 = 7,4
La HLB calculée indique que cet émulsifiant pourra être utilisé pour stabiliser une émulsion eau dans huile. Il est à noter que la valeur de E dépond des indices n, m, p et q. Si ces derniers augmentent, E augmente également ce qui modifie la valeur de la HLB.
Méthode 3.
Une troisième méthode, également empirique, est utilisable pour le calcul de la HLB. Elle prend en compte les masses molaires des parties hydrophiles et la masse molaire de l’ester. Prenons l’exemple de l’ester suivant : CH3-(CH2)10-CO-O-(O-CH2-CH2)8-CH3, son HLB pourra être calculé par la relation suivante :
Une valeur de 13 correspond au HLB d’un détergent [1], voir annexe 1
Méthode 4.
Une quatrième méthode très simple d’emploi consiste à définir et d’affecter à chaque groupement fonctionnel la valeur de l’énergie libre de transfert des groupes lipophiles et hydrophiles de l’émulsifiant au niveau de l’interface. Ces valeurs ont calculées et tabulées par Davis et Lin [4], voir tableau en annexe 2. Dans ces conditions, la HLB peut être évaluée par l’équation suivante :
Les HLB de différents groupes classiques sont disponibles dans la littérature [5]. Les valeur de HLB comprises entre 1 et 6 s’apparentent typiquement à des tensioactifs hydrophobe qui donneront des émulsions de type eau dans l’huile, E/H. Les HLB supérieures à 10, ont un caractère hydrophile et stabiliseront des émulsions de type huile dans l’eau (H/E).
Le fait que les HLB soient linéairement additifs, on peut facilement envisager de préparer des mélanges de tensioactifs pour réaliser des formulations stables. Lorsque l’on affaire à une valeur spécifique de HLB et qu’aucun tensioactif seul ne peut la fournir on aura recours à des combinaisons consistant à mélanger deux tensioactifs différents permettant, en vertu du principe d’additivité des HLB, d’obtenir la valeur de la HLB requise à l’aide de la relation :
Application numérique : détermination de HLB d’un mélange de deux tensioactifs
Considérons deux tensioactifs Span 60 et Tween 60 de HLB de 4,5 et 14,9 respectivement. A partir de ces données, on souhaite préparer une émulsion ayant une HLB de 7.5.
Solution. En appliquant l’équation (4) :
7,5 = 4.5 X1 + 14,9 X2 (a)
Avec X1 et X2 les pourcentages respectifs des tensioactifs 1 et 2
Sachant que X1 + X2 = 1 ou 100%
D’où, X2 = 1 – X1 (b)
En injectant la valeur de X2 l’expression ci-dessus, il devient possible de calculer aisément les pourcentages de X1 et X2 :
X1 = 0,27 ou 27% et X2 = 0.73 ou 73%
X1 et X2 représentent la composition du mélange de tensioactifs donnant une HLB de 7,5 recherchée.
Toutefois, il faut noter, que les valeurs attribuées aux groupements, hydrophiles et lipophiles, ne sont pas validées par certains articles scientifiques en raison de leur caractère empirique. Par ailleurs, un certain nombre de groupements n’ont pas été quantifiés. Malgré cette réserve, les méthodes proposées pour le calcul de la HLB restent très pratiques classer émulsifiants et orienter leurs emplois. Les émulsifiants commerciaux sont généralement des mélanges de molécules.
Conclusion
Notre article, en deux parties, fait le point sur une famille de produits chimiques, qualifiés de produits auxiliaires en ennoblissement textiles. Les tensioactifs sont utilisés comme agents mouillants, détergents, antimousses etc. Leurs emplois s’étendent au-delà de cette industrie. Une classification des agents de surface traités dans cet article a été effectuée sur la base de données bibliographiques. La classification des agents de surface s’appuie sur la nature de la fonction chimique responsable de la modification de la tension de surface. Dans la seconde partie de cet article, nous avons présenté les méthodes de calcul de la balance hydrophile-lipophile qui oriente l’utilisation du tensioactif vers l’application souhaitée.
Références bibliographiques
- Poré ‘’ Les dispersions Aqueuses, Ed. Le cuir, 1976
- Bourrel, ‘’ Tensioactifs en Solution, Interfaces et Micelles, Conférences, U. Bordeaux I 1983
- Griffin WC, Classification of Surface-Active Agents by HLB, Journal of the Society of Cosmetic Chemists 1 (1949)
- Davies JT, A quantitative kinetic theory of emulsion type, I. Physical chemistry of the emulsifying agent, Gas/Liquid and Liquid/Liquid Interface. Proceedings of the International Congress of Surface Activity (1957): 426-438
Annexes
Tableau-I
|
Spécificité du tensioactif |
Valeurs des HLB |
|
|
minimales |
maximales |
|
|
Antimousse |
1,5 |
3 |
|
Emulsion eau dans l’huile |
3 |
6 |
|
Mouillant |
7 |
9 |
|
Emulsion huile dans l’eau |
8 |
13 |
|
Détergent |
13 |
15 |
|
Dispersant -solubilisant |
15 |
18 |
Annexe 1- Classification des agents de surface en fonction de leurs HLB
Tableau-II
|
Groupe hydrophiles |
Valeur attribuée au groupement |
Groupement hydrophobe |
Valeur attribuée au groupement |
|
-O- |
1,3 |
=CH- |
-0,475 |
|
-OH libre |
1,9 |
-CH2- |
-0,475 |
|
-OH du sorbitol |
0,5 |
-CH3- |
-0,475 |
|
-COOH |
2,1 |
-CH2CH2CH2-O- |
-0,15 |
|
-COONa |
19,1 |
-CH(CH3)-CH2-O- |
-0,125 |
|
-CH2-CH2-O- |
0,35 |
Phényl |
-0,166 |
Annexe 2-Energie libre de transfert-de Davis et Lin